
核准日期:2007年04月05日
修改日期:2008年09月26日
修改日期:2012年10月31日
修改日期:2015年12月01日
修改日期:2019年12月01日
修改日期:2021年05月08日
盐酸二甲双胍缓释片说明书
请仔细阅读说明书并在医师指导下使用
【药品名称】
通用名称:盐酸二甲双胍缓释片
商品名称:倍顺
英文名称:Metformin Hydrochloride Sustained-release Tablets
汉语拼音:Yansuan Erjiashuanggua Huanshi Pian
【成份】
本品主要成份为盐酸二甲双胍。
化学名称:1,1-二甲基双胍盐酸盐
化学结构式:
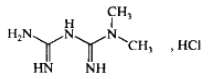
分子式: C4H11N5·HCl
分子量:165.63修改日期:2012年10月31日
修改日期:2015年12月01日
修改日期:2019年12月01日
修改日期:2021年05月08日
盐酸二甲双胍缓释片说明书
请仔细阅读说明书并在医师指导下使用
【药品名称】
通用名称:盐酸二甲双胍缓释片
商品名称:倍顺
英文名称:Metformin Hydrochloride Sustained-release Tablets
汉语拼音:Yansuan Erjiashuanggua Huanshi Pian
【成份】
本品主要成份为盐酸二甲双胍。
化学名称:1,1-二甲基双胍盐酸盐
化学结构式:

分子式: C4H11N5·HCl
辅料为:羟丙甲纤维素,羧甲纤维素钠,微晶纤维素和硬脂酸镁。
【性状】
本品为白色或类白色片。
【适应症】
本品用于单纯饮食控制及体育锻炼控制血糖无效的成人2型糖尿病,可以单药治疗,也可以与磺脲类药物或胰岛素联合。
【规格】0.5g
【用法用量】
必须整片吞服,不得碾碎或咀嚼后服用。
为了减少胃肠道并发症的发生,也为了使用最小剂量的药物使患者的血糖足以控制,应从小剂量开始服用,逐渐增加剂量。
治疗开始和调整剂量期间(见推荐的服药计划),测定空腹血糖可用于确定本品治疗反应,以及确定患者最小的有效剂量。此后,应每隔三月测定糖化血红蛋白。无论是单独使用还是与磺脲类药物及胰岛素联合使用,治疗的目标都是使用最低的有效剂量使空腹血糖和糖化血红蛋白水平降至正常或接近正常水平。
推荐服药计划
肾功能正常(eGFR≥90mL/min/1.73m2)的成人
单药治疗以及与其它口服降糖药联合治疗
通常盐酸二甲双胍缓释片的起始剂量为500毫克,1次/日随晚餐服用,每周剂量增加500毫克,最大剂量至2000毫克,1次/日随晚餐服用。如果用至2000毫克,1次/日,血糖仍没有控制满意,可以考虑改用1000毫克,2次/日随餐服用。如果还需要更大量的二甲双胍,应当使用盐酸二甲双胍片2550毫克/日的最大剂量,分次服用。
一项使用盐酸二甲双胍片治疗的患者转变为盐酸二甲双胍缓释片实验结果提示,接受盐酸二甲双胍片治疗的患者可以安全的以相同剂量转换为盐酸二甲双胍缓释片1次/日的治疗,最高至2000毫克,1次/日。转变后要严密监测血糖,并相应调整剂量。
从其他降糖治疗转变治疗
除了氯磺丙脲,患者从其他的口服降糖药转为本品治疗时通常是不需要转换期。服用氯磺丙脲的患者在换用本品的最初2周要密切注意,因为氯磺丙脲在体内滞留时间长,易导致药物作用过量,发生低血糖。
与磺脲类药物联合使用
如果服用最大推荐剂量的本品数周后仍无反应的患者,应当考虑在维持最大剂量治疗的同时逐渐加用磺脲类口服降糖药物,除非患者已存在对磺脲类药物原发或继发失效。目前仅有二甲双胍与格列本脲(优降糖)之间相互作用的临床和药代动力学的数据。
联合服用本品与磺脲类药物,通过调整两种药物的剂量可以达到满意的血糖控制。联合本品治疗,磺脲类药物发生低血糖的危险性持续存在,甚至有所增加,应当进行恰当的预防。(见所选择的磺脲类药物的包装说明)
如果患者联合最大剂量的本品与最大剂量的口服磺脲类药物治疗1至3个月仍不能满意控制血糖,要考虑改变治疗方法,包括联合本品胰岛素治疗或胰岛素单独治疗。
与胰岛素在成人中联合使用
开始加用本品时可以维持胰岛素的剂量。胰岛素治疗的患者本品起始剂量应为500毫克,1次/日。如果患者的反应不够时,1周后增加500毫克,此后可以每周增加500毫克直到达到满意的血糖控制。推荐的每日最大剂量是2000毫克。当联合使用本品与胰岛素的患者的空腹血糖降至120mg/dL以下时,建议减低胰岛素剂量的10%~25%。应当根据血糖降低的反应继续进行个体化的调整或遵医嘱。
肾功能受损患者的剂量调整
eGFR≥60mL/min/1.73m2无需调整剂量,eGFR 45~59mL/min/1.73m2减量,eGFR<45mL/min/1.73m2禁用。
【不良反应】据国外文献报道:
初始治疗时,最常见的不良反应有恶心、呕吐、腹泻、腹痛和食欲不振,大多数患者通常可以自行缓解。
以下不良反应可能在服用盐酸二甲双胍缓释片时出现。
不良反应发生频率定义如下:十分常见(≥10%),常见(1%~10%,含1%) ,偶见(0.1%~1%,含0.1%),罕见(0.01%~0.1%,含0.01%),十分罕见(<0.01%)。
每个频率组中,不良反应是按照严重程度递减的顺序排列的。
代谢和营养障碍:
十分罕见:
- 乳酸酸中毒(见【注意事项】)
- 长期服用二甲双胍可能减少维生素B12的吸收。若患者出现巨幼红细胞贫血时应考虑该原因。
常见:
- 味觉障碍
十分常见:
- 胃肠道异常例如恶心、呕吐、腹泻、腹痛和食欲不振。这些不良反应大多发生在开始治疗时,大多数患者通常可以自行缓解。缓慢增加剂量可提高胃肠道耐受性。
十分罕见:
- 有肝功能检查异常或肝炎的个别病例在停止服用二甲双胍后恢复正常的报告。
十分罕见:
- 皮肤反应,例如红斑、瘙痒、荨麻疹。
【禁忌】
- 严重的肾功能衰竭(eGFR<45mL/min/1.73m2);
- 可能影响肾功能的急性病情,如:脱水、严重感染、休克;
- 可造成组织缺氧的疾病(尤其是急性疾病或慢性疾病的恶化),例如失代偿性心力衰竭、呼吸衰竭、近期发作的心肌梗死和休克;
- 严重感染和外伤,外科大手术,临床有低血压和缺氧等;
- 已知对盐酸二甲双胍和本品中任何成份过敏;
- 任何急性代谢性酸中毒,包括乳酸酸中毒、糖尿病酮症酸中毒;
- 糖尿病昏迷前驱期;
- 肝功能不全、急性酒精中毒、酗酒;
- 维生素B12、叶酸缺乏未纠正者。
乳酸酸中毒:
乳酸酸中毒是一种非常罕见但严重的代谢并发症,可由于二甲双胍在体内蓄积而诱发,常见于肾功能急性恶化、患有心肺疾病或败血症的患者中。
出现脱水(严重腹泻或呕吐、发热或液体摄入量减少)的患者应暂时停用二甲双胍并告知医生。
在服用二甲双胍患者中,应警惕使用可以引起肾功能急性受损的药物【包括降压药、利尿剂和非甾体类抗炎药(NSAIDs)】。乳酸酸中毒的风险因素还包括过量饮酒、肝功能不全、糖尿病控制不佳、酮症、长期禁食和任何可能引起缺氧的疾病,以及同时使用可能引起乳酸酸中毒的药物。
应告知患者和/或看护者乳酸酸中毒的风险。乳酸酸中毒的特点为酸中毒呼吸困难、腹痛、肌肉痉挛、衰弱和体温降低,进而昏迷。一旦出现可疑症状,患者应立即停用二甲双胍并及时告知医生。实验室检查异常包括pH值降低(<7.35)、血浆乳酸水平高于5mmol/L和阴离子间隙以及乳酸/丙酮酸比值升高。
乳酸酸中毒是必须在医院治疗的急症。服用本品的乳酸酸中毒患者应立即停药并及时进行支持诊断的检查。
一般注意事项
肾功能:
慢性肾脏病变是糖尿病的常见并发症,一旦确诊糖尿病,应常规检查肾功能。二甲双胍经过肾脏排泄,随着肾功能受损的程度的增加,二甲双胍蓄积和发生乳酸酸中毒的危险性随之增加。开始治疗前以及治疗后应至少每年检查肾功能。
本品禁用于eGFR<45mL/min/1.73m2的患者。出现脱水、严重感染或休克等影响肾功能的急性病情的患者应暂时停用本品。(见【禁忌】)
心功能:
心衰患者缺氧和肾功能不全的风险更高。稳定性慢性心衰的患者在定期检查心、肾功能的情况下可以服用二甲双胍。
二甲双胍禁用于急性和不稳定性心衰的患者(见【禁忌】)。
碘化造影剂的使用:
向血管内注射碘化造影剂可能导致造影剂肾病,这可能引起二甲双胍蓄积和增加乳酸酸中毒的风险。因此,计划做这类检查的患者,在检查前或检查时必须停止服用二甲双胍,在检查完成至少48小时后且仅在再次检查肾功能稳定的情况下才可以恢复用药。
外科手术:
在接受常规、脊髓或硬膜外麻醉的手术时必须停止服用二甲双胍。术后至少48小时或恢复进食并且肾功能经评估稳定后才可以重新开始治疗。
其他注意事项:
所有患者应继续合理安排碳水化合物的饮食摄入。超重患者应继续热量限制性饮食。
应定期进行常规实验室检查以监测糖尿病。
维生素B12水平——某些患者(那些摄入或吸收维生素B12和钙不足的患者)可能更容易发生维生素B12水平的降低。这种患者每隔2-3年测定一次血清维生素B12水平是有益的。
低血糖——单独接受本品治疗的患者正常情况下不会产生低血糖,但与胰岛素或其他降糖药物(例如磺脲类药物或格列奈类药物)联合使用应警惕低血糖。
老年、衰弱或营养不良的患者,以及肾上腺和垂体功能低减、酒精中毒的患者更易发生低血糖。
【孕妇及哺乳期妇女用药】
孕妇
对于计划怀孕或已经怀孕的患者,不推荐使用二甲双胍,但可以使用胰岛素来维持血糖水平,使其尽可能接近正常水平,从而降低胎儿畸形的风险。
哺乳期妇女
二甲双胍可以通过乳汁排泄。在二甲双胍治疗期间不推荐哺乳。
【儿童用药】
儿童(17岁以下)使用本品的安全性和疗效尚未建立,暂不推荐使用。
【老年用药】
由于老年患者可能出现肾功能减退,应定期检查肾功能并根据肾功能进行调整二甲双胍的剂量。
【对驾驶和操作机械的能力的影响】
单独接受二甲双胍治疗的患者正常情况下不会产生低血糖,因此二甲双胍对驾驶和操作机械的能力没有影响。但与胰岛素或其他降糖药物(例如磺脲类药物或格列奈类药物)联合使用应警惕低血糖。
【药物相互作用】
1. 单剂联合使用二甲双胍和格列本脲未发现二甲双胍的药代动力学参数改变。
2. 二甲双胍与呋塞米(速尿)合用,二甲双胍的AUC增加,但肾清除无变化;同时呋塞米的Cmax和AUC均下降,终末半衰期缩短,肾清除无改变。
3. 经肾小管排泌的阳离子药物(例如氨氯吡咪、地高辛、吗啡、普鲁卡因胺、奎尼丁、奎宁、雷尼替丁、氨苯喋啶、甲氧苄氨嘧啶和万古霉素)理论上可能与二甲双胍竟争肾小管转运系统,发生相互作用,因此建议密切监测,调整本品及/或相互作用的药物剂量。
4. 二甲双胍与西咪替丁合用,二甲双胍的血浆和全血AUC增加,但两药单独合用,未见二甲双胍清除半衰期改变。西咪替丁的药代动力学未见变化。
5. 如同时服用某些可引起血糖升高的药物,如噻嗪类药物或其他利尿剂、糖皮质激素、吩噻嗪、甲状腺制剂,雌激素、口服避孕药、苯妥英、烟碱酸、拟交感神经药、钙离子通道阻滞剂和异烟肼等时要密切监测血糖,而在这些药物停用后,要密切注意低血糖的发生。
6. 二甲双胍不与血浆蛋白结合。因此与蛋白高度结合的药物,如水杨酸盐、氨苯磺胺、氯霉素、丙磺舒等与磺脲类药物相比不易发生相互作用,后者主要与血清蛋白结合。
7. 除氯磺丙脲,患者从其他口服降糖药转为用本品治疗时,通常不需转换期。服用氯磺丙脲的患者在换用本品的最初2周要密切注意,因为氯磺丙脲在体内有较长滞留,易导致药物作用过量,发生低血糖。
8. 健康人单剂联合使用硝苯地平和二甲双胍,二甲双胍的血浆峰浓度和血浆浓度时间曲线下面积分别增加20%和9%,且尿中排泄增加,Tmax和半衰期无影响。
9. 二甲双胍有增加华法林的抗凝血倾向。
10. 树脂类药物与本品合用,可减少二甲双胍吸收。
【药物过量】
即使二甲双胍服药量达到85克都没有发生低血糖,但在这种情况下会发生乳酸酸中毒。在良好的血液动力学的状况下二甲双胍可以以170mL/min的速度透析清除。因此怀疑二甲双胍过量的患者,血透可以清除蓄积的药物。
【药理毒理】
药理作用
二甲双胍可减少肝糖生成,抑制葡萄糖的肠道吸收,并增加外周组织对葡萄糖的摄取和利用,可通过增加外周糖的摄取和利用而提高胰岛素的敏感性。
毒理研究
遗传毒性
本品Ames试验、小鼠淋巴细胞基因突变试验、人淋巴细胞染色体畸变试验和小鼠微核试验结果均为阴性。
生殖毒性
雄性大鼠和雌性大鼠给予盐酸二甲双胍,剂量高达600mg/kg/日(按体表面积折算相当于人临床推荐最大日剂量的3倍),未见对生育能力的影响。大鼠和兔给予盐酸二甲双胍,剂量高达600mg/kg/日(按体表面积折算相当于人临床推荐最大日剂量的2倍和6倍)时,无致畸胎作用。哺乳期大鼠的研究结果显示,盐酸二甲双胍可分泌入乳汁,并可达到在血浆的水平。
致癌性
大鼠给予二甲双胍900 mg/kg/日104周,小鼠给予二甲双胍1500 mg/kg/日91周致癌性研究(这些剂量按体表面积计算相当于二甲双胍临床每日最大推荐剂量2000mg的4倍),雄性和雌性小鼠中均未发现二甲双胍致癌作用的证据。二甲双胍在雄性大鼠中也未发现致癌作用,但在900 mg/kg/日的雌性大鼠中,有良性间质子宫息肉发生率的增加。
【药代动力学】据国外文献报道:
吸收:
口服二甲双胍缓释片与二甲双胍速释片相比,二甲双胍的吸收时间明显延长,血药浓度在7小时(Tmax)后达到峰值(Cmax)(二甲双胍速释片的Tmax是2.5小时)。达到稳态时,与二甲双胍速释片相似,二甲双胍缓释片的Cmax和AUC与口服剂量不成比例。单剂量口服二甲双胍缓释片2000mg的AUC与二甲双胍速释片1000mg bid的AUC相似。
二甲双胍缓释片的Cmax和AUC的个体间差异与二甲双胍速释片相似。
在空腹状态下口服二甲双胍缓释片,AUC减少30%(Cmax和Tmax不受影响)。
二甲双胍缓释片的吸收程度不受食物成份影响。
多次口服二甲双胍缓释片2000mg后未观察到二甲双胍蓄积。
分布:
二甲双胍几乎不与血浆蛋白结合。二甲双胍部分进入红细胞。二甲双胍全血浓度峰值低于血浆浓度峰值,但出现时间大致相同。红细胞可能是二甲双胍的第二分布腔室,平均分布容积(Vd)在63-276L之间。
代谢:
二甲双胍主要以原型从尿液排出。在人体中未检测到相关代谢产物。
排泄:
二甲双胍的肾脏清除率>400mL/min,提示肾小球滤过和肾小管分泌是二甲双胍排泄的途径。口服给药后,二甲双胍的终末血浆清除半衰期约为6.5小时。
肾功能不全时,肾脏清除率会随肌酐清除率下降而下降,因此二甲双胍的清除半衰期延长,导致血浆二甲双胍浓度上升。
在特殊人群中的特征
肾功能不全
目前在中度肾功能不全患者中治疗的数据较少,且在这些人群中也没有与肾功能正常患者比较的二甲双胍全身暴露量的可靠估计。因此,应考虑临床疗效/耐受性以调整剂量。
【贮藏】密封保存。
【包装】
铝塑包装(聚氯乙烯固体药用硬片/药用铝箔)
10片/板×1板/盒,10片/板×2板/盒,10片/板×3板/盒,10片/板×4板/盒。
【有效期】24个月
【执行标准】YBH14682020
【批准文号】国药准字H20030952
【药品上市许可持有人】
名称:成都恒瑞制药有限公司
注册地址:成都高新区西部园区百草路18号
邮政编码:611731
电话号码:028-87846099
传真号码:028-87848309
网址:http://www.santao.com.cn
【生产企业】
企业名称:成都恒瑞制药有限公司
生产地址:成都高新区西部园区百草路18号
邮政编码:611731
电话号码:028-87846099
传真号码:028-87848309
网址:http://www.santao.com.cn
